文:羅浚晅醫師、林建廷醫師(卡洛生醫團隊)
前言:從控制疾病到追求治癒的典範轉移
在風濕免疫學的發展史上,經歷了從早期類固醇、免疫抑制劑進步到近代生物製劑(biologics)的巨大跨越,在疾病照護上增加不少治療利器。然而,對於不少嚴重的紅斑性狼瘡(SLE)、全身性硬化症(SSc,硬皮症)或多發性肌炎的患者而言,醫學的進步只是將「死刑」改為「無期徒刑」。患者往往必須終身服用藥物,忍受藥物帶來的副作用,並擔心病情隨時可能的反撲。
近年來,原本在血液癌症領域大放異彩的CD19 CAR-T(嵌合抗原受體 T 細胞)或BCMA CAR-T療法,正以一種「破壞式創新」的姿態快速進入自體免疫領域,讓醫界看到了一個前所未有的可能性:免疫重置(Immune Reset)。這不再只是壓制免疫系統,而是透過「清除與重建」,讓患者有機會徹底擺脫藥物,回歸正常生活。
第一部分:何謂 CAR-T?改裝免疫系統的精準導彈
CAR-T 療法的核心在於「自體武裝」。醫師先從患者體內採集自體T細胞,透過基因工程技術,在實驗室中為這些T細胞安裝導航系統,也就是嵌合抗原受體(CAR)。詳細的介紹可參考本系列之前的文章。
這個 CAR 分為兩個重要部分:
1.細胞外結合域:像是一把精準的鑰匙,專門尋找目標細胞表面的特定「鎖」(抗原)。
2.細胞內信號域:一旦鎖定目標,便會啟動 T 細胞的攻擊開關,將目標細胞殲滅。
回輸病人體內的CAR-T細胞不僅會發動攻擊,還會在患者體內自我增殖,形成一支強大的免疫軍隊。在血液腫瘤中,這支軍隊負責清理癌細胞;而在自體免疫疾病中,CAR-T的任務是消滅那些產生「錯誤自體抗體」的細胞,主要是B細胞或漿細胞(plasma cell)。
第二部分:為何BCMA是攻克自體免疫的關鍵?
在自體免疫疾病的CAR-T治療中,CD19是最早開發的靶點。然而,隨着研究深入,科學家發現CD19雖然能清除大部分B細胞,卻難以撼動真正的大型抗體生產基地。
1.B細胞與漿細胞的區別
B細胞是免疫系統中的預備兵。當它們接收到刺激後,會發育成為漿細胞。漿細胞才是真正負責大量分泌抗體的工廠,可參考<圖一>。
- CD19靶點:廣泛存在於各階段的B細胞,但僅僅微量存在於最早期的漿母細胞(plasmablast),並且不存在於最成熟的漿細胞。
- BCMA靶點:主要且高度表達在成熟漿細胞上,甚至可微量存在於晚期的B細胞上。
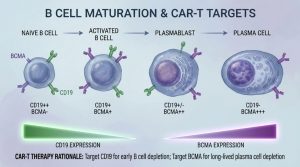
2.直擊長壽漿細胞(long-lived plasma cell)
在狼瘡腎炎、硬皮症、或重症肌無力的重症患者體內,最致病、最難纏的自體抗體往往是由「長壽漿細胞」持續產生的。這些漿細胞躲藏在骨髓中,對傳統的免疫抑制劑、甚至CD19 CAR-T具有抗性。BCMA CAR-T的出現,填補了這一重大缺口,BCMA CAR-T能精準識別並摧毀這些持續製造異常自體抗體的漿細胞,從源頭阻斷致病抗體的產生。
第三部分:臨床實證– 從10公尺到10公里的生命奇蹟
德國德蘭斯登大學(University of Erlangen-Nuremberg)的Georg Schett教授是將 CAR-T引入自體免疫領域的靈魂人物。從他的研究中,我們看到了令人震撼的轉變。
1.免疫重置的實證
Schett教授觀察到,自體免疫疾病患者在接受CAR-T治療後,體內的致病抗體會在3個月內迅速消失。最神奇的是,當CAR-T細胞完成任務逐漸消退後,患者體內會重新長出新的B細胞。然而,這些「新生代」B 細胞表現得非常規矩,不會再攻擊自身組織。這證明了CAR-T能夠將混亂的免疫系統「重開機」並恢復正常運作。
2.跨疾病的廣泛療效
根據 2025 年末發布的Spherix Global Insights報告與相關臨床試驗:
- 全身性硬化症(SSc):這是一種最令醫師頭痛的疾病,患者的皮膚與內臟會不斷纖維化(變硬)。最新數據顯示,BCMA CAR-T治療後,患者的肺功能指標不僅停止惡化,甚至出現了改善。這在過去的醫學紀錄中是極為罕見的。
- 系統性紅斑狼瘡(SLE)與狼瘡腎炎:估計在台灣約有 2.4 萬名患者罹患SLE。過去對於難治型SLE重症,醫師幾乎束手無策,藥物極其有限。現在,BCMA CAR-T 有機會讓幾乎失去社交生活能力的患者,能夠重新回到職場。
- 特發性發炎性肌炎(IIM):患者原本肌肉無力到無法行走。在治療後,可以恢復運動能力,正如 Müller 醫師所說:「他們曾經幾乎無法走十公尺,現在卻能夠走上十公里路!」
第四部分:挑戰與爭議–革命性技術的代價
儘管前景輝煌,但BCMA CAR-T並非沒有風險。在 2026年初的風濕病專家調查中,高達 68% 的醫師對其風險與益處的平衡仍持觀望態度。
1.細胞激素釋放症候群(CRS)
當CAR-T大舉進攻時,會釋放大量的發炎因子。這會導致患者可能出現高燒、低血壓甚至器官衰竭。所幸在自體免疫疾病患者中,CRS的嚴重度通常大幅度低於癌症患者,因此安全性好很多,但仍需進行必要的監控。
2.免疫空窗期與感染風險
清除漿細胞意味着清除體內幾乎所有的抗體工廠。這會導致患者處於「低免疫球蛋白血症(Hypogammaglobulinemia)」的狀態持續一段時間,而在此階段相對易受到肺炎、帶狀皰疹等病原體的侵襲。這需要醫師在治療後進行細緻的抗體補充與感染預防,靜待正常的漿細胞恢復。
3.天價成本與可及性
目前CAR-T的治療費用高達800萬至1500萬台幣。對於大多數家庭而言,這是一個天文數字。如何讓這項藥物平民化,是未來幾年健保政策與製藥產業最大的挑戰之一。
第五部分:未來展望–CAR-T的 2.0 時代
為了克服目前的瓶頸,科學界正發展出多種優化方案:
1.雙重靶點策略(Dual-targeting):目前已發展出CD19/BCMA雙靶點CAR-T。這就像是雙重防線,CD19主責清理B細胞,BCMA主責清理漿細胞,確保不留任何死角。
2.現貨通用型CAR-T(Allogeneic CAR-T):目前的治療需要因病人量身訂做,耗時且昂貴。未來,科學家希望利用健康捐贈者的細胞,大規模生產通用型的CAR-T產品,讓患者像其他藥物一樣隨到隨用,並將價格壓低。
3.門診化與免除淋巴清除治療:透過改進甚至免除淋巴清除化療方案(lymphodepletion),希望能讓患者不需要住院,而是在門診就能完成CAR-T輸注。
結語:我們正在見證歷史
從2024年周海媚遺憾離世引起社會對狼瘡的關注,到2026年BCMA CAR-T逐漸展現出驚人療效,我們正站在一個醫學時代的交界處。
BCMA CAR-T的意義,不僅僅是多了一種強效藥物,而是挑戰了我們對慢性病的定義。當抗體工廠被精準摧毀,當免疫系統被徹底重啟,我們或許可以大膽地預測:在不久的未來,自體免疫疾病將不再是患者沉重的終身枷鎖,而是一段可以被重置與改寫的人生經歷。
正如風濕學界所期待的,我們需要的不再是更多的壓制,而是一次精準的免疫重啟。這台名為CAR的車,正載着成千上萬的患者,駛向一個不再需要恐懼的明天。
本文僅代表作者立場,不代表本平台立場









Facebook Comments 文章留言